Veterinary Clinics of North America: Small Animal Practice
May 2017
Перевод с англ.: ветеринар - невролог/кардиолог Васильев
Ключевые моменты
- Клиницисты должны знать, что признаки печеночной энцефалопатии у собак и кошек могут быть едва заметными и периодическими.
- Аммиак – не единственный фактор, вызывающий печеночную энцефалопатию; имеются убедительные доказательства того, что воспаление также играет ключевую роль. Знание этих других факторов и предрасполагающих факторов улучшает ведение таких случаев.
- Ограничение потребления белка в рационе больше не является краеугольным камнем в лечении печеночной энцефалопатии.
Введение
Гепатоэнцефалопатия наиболее часто определяется в ветеринарии как неврологическая дисфункция, вызванная заболеванием печени и/или портосистемным шунтированием. Это определение учитывает различные последствия заболевания печени для центральной нервной системы, которые необходимо охватить. В медицине человека определены широкие категории заболеваний печени, приводящих к печеночной энцефалопатии, и они применимы в ветеринарии (таблица 1). В ветеринарии, хотя острая гепатопатия встречается нередко, из-за резервных возможностей печени острая печеночная недостаточность (категория А) является относительно редкой причиной печеночной энцефалопатии у собак и кошек. Категория В является наиболее распространенной причиной печеночной энцефалопатии, наблюдаемой в ветеринарной практике, из-за высокой распространенности врожденных портосистемных шунтов. Для животных-компаньонов было предложено расширить категорию С, включив в нее все хронические заболевания печени, а не только конечную стадию цирроза.
Клинические симптомы
Спектр клинических симптомов варьирует от едва заметных отклонений в поведении до комы. При гепатоэнцефалопатии могут возникать судорожные припадки, хотя они обычно встречаются в сочетании с несколькими симптомами, а не изолированно. Шкала оценок тяжести заболевания для людей модифицирована для ветеринарных пациентов (таблица 2). В медицине для людей используется более тонкая оценка: минимальная печеночная энцефалопатия, при которой люди кажутся неврологически нормальными, но при психометрическом тестировании выявляются когнитивные нарушения.
Было высказано предположение, что человеческая шкала будет пересмотрена, объединив нулевую и первую степень отчасти из-за субъективности в точном определении первой степени. Они будут объединены в “скрытую печеночную энцефалопатию ” и II-IV степени, называемую “явной печеночной энцефалопатий ”. Маловероятно, что, имеет смысл определения нулевой степени у собак и кошек. Однако, вероятно, что определение I степени в ветеринарной медицине страдает повышенной субъективностью; в рамках консультации снижение умственной активности является относительным понятием, а сопутствующие заболевания (например, дегенеративное заболевание суставов у собаки с хроническим гепатитом) могут способствовать апатии. Следовательно, возможно, что животные I степени могут быть классифицированы как бессимптомные и наоборот. Клинические признаки печеночной энцефалопатии часто усиливаются и ослабевают, при этом животные переходят от симптоматического к асимптомному течению.
Хроническиая печеночная энцефалопатия может быть подразделена на постоянную или эпизодическую (см. таблицу 1). Поскольку клинические признаки могут быть малозаметными и проявляться эпизодически, врачам следует поддерживать высокий уровень подозрительности у животных, подверженных риску печеночной энцефалопатии. Нераспознанная печеночная энцефалопатия может способствовать заболеваемости и, в конечном счете, смертности из-за снижения качества жизни. Владельцы часто, на удивление, не замечают, когда у их животного проявляются явные отклонения в поведении, как у молодых животных с врожденными портосистемными шунтами, так и у пожилых животных с приобретенными шунтами. Обучение владельцев помогает справиться с этим заболеванием, особенно в случаях эпизодической печеночной энцефалопатии.
Таблица 1. Категория патологического процесса печени, приводящего к печеночной энцефалопатии, с рекомендуемой ветеринарной модификацией
Таблица 2. Ветеринарная модификация Вест-Хейвенской шкалы оценки печеночной энцефалопатии
Тип гепатоэнцефалопатии
Острая гепатоэнцефалопатия
Она проявляется при острой печеночной недостаточности и является частью совокупности клинических признаков, которые включают быстрое и прогрессирующее ухудшение состояния. У животных часто наблюдаются множественные метаболические/биохимические нарушения, такие как нарушения электролитного баланса или кислотно-щелочного баланса, которые способствуют клиническому проявлению и гипераммониемии. Печеночная энцефалопатия протекает в тяжелой форме, животные часто впадают в ступор или кому (III/IV степень печеночной энцефалопатии). Эти пациенты нуждаются в интенсивном лечении (о котором речь пойдет позже), и прогноз у них неблагоприятный.
Хроническая гепатоэнцефалопатия
Это наиболее распространенная форма заболевания в ветеринарии, вызываемая врожденным или приобретенным портосистемным шунтированием. Хотя были описаны случаи печеночной энцефалопатии при хронических заболеваниях печени, когда шунтирующий сосуд не был идентифицирован, это, скорее всего, вызвано недостаточной чувствительностью тестов для определения этих сосудов, поскольку печень обладает таким большим резервным потенциалом, что изолированная хроническая печеночная недостаточность как причина печеночной энцефалопатии маловероятна.
Факторы, принимающие участие в патогенезе печеночной энцефалопатии
Многие метаболические нарушения, которые могут возникать вследствие заболеваний печени, могут оказывают влияние на центральную нервную систему. Прошло более 100 лет с тех пор, как Nencki и его коллеги описали и исследовали его патогенез у собак с использованием хирургически созданных портосистемных шунтов. Их новаторская работа продемонстрировала, что печень преобразует аммиак в мочевину, а поступление аммиака в системный кровоток и, в конечном счете, в центральную нервную систему приводит к неврологическим нарушениям.
Бесспорно, что аммиак играет центральную роль в патогенезе печеночной энцефалопатии; однако в медицине человека и ветеринарии уже давно признано, что, хотя в популяции людей с хронической печеночной энцефалопатией существует корреляция между содержанием аммиака и уровнем печеночной энцефалопатии, концентрация аммиака является плохим прогностическим фактором печеночной энцефалопатии у человека. В медицине человека печеночная энцефалопатия является скорее диагнозом исключения, чем результатом измерения содержания аммиака. Это привело к проведению клинических и экспериментальных исследований, направленных на понимание того, какие другие факторы важны в патогенезе печеночной энцефалопатии, и концепции синергизма с аммиаком. Было выдвинуто предположение, что многие факторы могут усиливать печеночную энцефалопатию наряду с аммиаком, и в настоящее время наиболее убедительные доказательства имеются для наличие воспаления и марганца (изобр 1).
Аммиак
В настоящее время считается, что большая часть аммиака, образующегося в желудочно-кишечном тракте, образуется в результате преобразования энтероцитами глутамина в глутамат для получения энергии, с меньшей ролью уреаза – продуцирующих бактерий и деградации белка бактерий. Портальная кровь содержит аммиак в концентрациях, которые могут быть нейротоксичными при попадании непосредственно в системный кровоток.
- Детоксикация аммиака в печени
У здоровых животных печень является основным органом детоксикации аммиака. Это достигается двумя основными механизмами. Перипортальные гепатоциты преобразуют аммиак в мочевину через цикл образования мочевины. Мочевина значительно менее токсична и выводится почками. Некоторое количество мочевины подвергается кишечно-печеночной рециркуляции через слюну, желчь или непосредственно диффузией в желудочно-кишечный тракт, где она разлагается бактериями, продуцирующими уреазу. По мере того, как кровь поступает в центрально-дольковую вену, происходит переключение процессов детоксикации аммиака на превращение глутамата в глутамин с помощью фермента глутаминсинтетазы, при этом потребляется аммиак.
Этот переход происходит постепенно через печеночную дольку, таким образом, что перивенозные гепатоциты в основном используют глутамат/глутаминовый путь. Детоксикация аммиака в печени чрезвычайно эффективна, поэтому кровь, поступающая в системный кровоток, содержит низкие концентрации аммиака. Существует большой резервный потенциал, и даже при тяжелой печеночной недостаточности детоксикация аммиака часто сохраняется. При портосистемном шунтировании, в зависимости от фракции шунтирования, различные доли крови с высокой концентрацией аммиака в портальных сосудах попадают непосредственно в системный кровоток.
- Метаболизм аммиака в почках
Почки играют решающую роль в защите организма от гипераммониемии посредством выведения мочевины и аммиака. Большая часть аммиака, который выводится с мочой, образуется в почках. В почках содержится глутаминаза, которая расщепляет глутамин, производя NH+ и HCO3- . Этот механизм важен для поддержания кислотно-щелочного гомеостаза; образующийся аммиак может либо попадать в системный кровоток, либо выводиться с мочой. Метаболический ацидоз увеличивает выведение аммиака с мочой, в то время как алкалоз и гипокалиемия увеличивают выработку аммиака почками, что потенцирует развитие печеночной энцефалопатии. Имеются данные о том, что выработка аммиака почками и выведение его с мочой могут увеличиваться при гипераммониемии.
- Метаболизм аммиака в скелетных мышцах
Скелетные миоциты содержат глютаминсинтетазу и, благодаря своей большой массе, обладают значительной способностью выводить аммиак путем превращения в глютамин. Однако это связывание аммиака носит временный характер, поскольку глутамин высвобождается в системный кровоток, где глутаминазы регенерируют аммиак и глутамат. Тем не менее, этот процесс может выступать в качестве важного буфера для устранения проблем с аммиаком.
- Метаболизм аммиака в центральной нервной системе и патогенез печеночной энцефалопатии
Астроциты - самые многочисленные клетки головного мозга, их доля составляет от 25% до 50% общего обьема мозга. Ключом к патогенезу печеночной энцефалопатии является дисфункция астроцитов. Эти клетки содержат фермент глутаминсинтетазу и действуют как буфер для повышения концентрации аммиака в центральной нервной системе. В результате концентрация глутамата снижается, а концентрация глутамина увеличивается. Глутамат является возбуждающим нейромедиатором, в то время как глутамин является тормозящим. Эти нейромедиаторы циркулируют между астроцитами и нейронами (изобр. 2). Глютамин высвобождается из астроцитов, поглощается нейронами и преобразуется в глутамат ферментом глутаминазой. Глутамат высвобождается в качестве нейромедиатора в синаптической щели. Астроциты быстро поглощают высвобожденный глутамат обратно. Высокие концентрации аммиака повышают уровень внеклеточного глутамина, препятствуя дальнейшему высвобождению из астроцитов, что приводит к повышению внутриклеточной концентрации.
Аммиак также ингибирует ключевые ферменты цикла трикарбоновых кислот, снижая способность астроцитов к аэробному дыханию, вызывая переключение на анаэробное дыхание и выработку лактата. Астроцитарные митохондрии катаболизируют глютамин, высвобождая аммиак, вызывающий окислительный стресс и митохондриальную дисфункцию. Эти метаболические эффекты приводят к набуханию астроцитов. Поскольку астроциты составляют значительную часть объема мозга, при острой печеночной энцефалопатии это приводит к отеку мозга и повышению внутричерепного давления. Этому также способствуют нарушения контроля мозгового кровотока. Это может быстро привести к образованию грыжи, сдавлению ствола мозга и смерти.
При хронической печеночной энцефалопатии набухание астроцитов менее выражено, но все еще присутствует, приводя к образованию астроцитов типа Alzheimer II. Именно такие случаи чаще всего встречаются в ветеринарной медицине, когда корреляция с концентрациями аммиака менее выражена, а другие факторы становятся более значимыми.
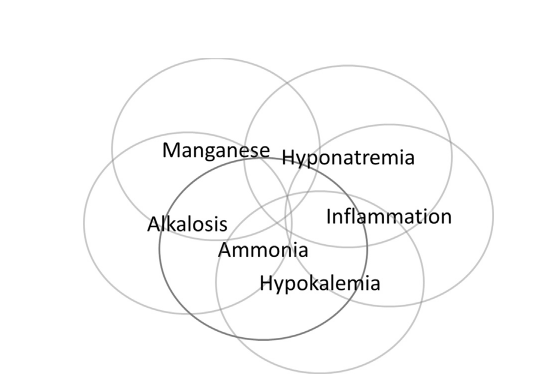
Изобр. 1 . Представление факторов, участвующих в патогенезе гепатоэнцефалопатии.
Воспаление
В настоящее время в медицине человека имеются убедительные доказательства того, что воспаление является важным потенцирующим фактором печеночной энцефалопатии. В подтверждение этого было показано, что крысы с экспериментально индуцированной печеночной энцефалопатией восстановили способность к обучению после введения нестероидных противовоспалительных препаратов. Было показано, что у собак с портосистемным шунтом уровень С-реактивного белка повышен у собак с признаками печеночной энцефалопатии и что аммиак и синдром системного воспалительного ответа позволяют прогнозировать наличие печеночной энцефалопатии Любой процесс, вызывающий системную воспалительную реакцию, потенциально может вызывать печеночную энцефалопатию. У собак с портосистемным шунтом наблюдается более высокая концентрация эндотоксинов в портальном и периферическом кровотоке, что позволяет предположить, что желудочно-кишечный тракт и микробиом могут быть важными движущими силами, и, в подтверждение этого, блокирование шунта приводит к снижению циркулирующих маркеров воспаления.
Провоспалительные цитокины усиливают мозговой кровоток и нарушают гематоэнцефалический барьер, повышая проницаемость для аммиака. Гематоэнцефалический барьер препятствует прямому проникновению системных цитокинов в центральной нервной системе. Однако цитокины все еще могут влиять на центральную нервную систему, возможно, через афферентные нервы; активный транспорт через гематоэнцефалический барьер; или через области, в которых гематоэнцефалический барьер отсутствует, такие как циркумвентрикулярные органы. Как медиаторы воспаления, так и аммиак вызывают активацию микроглии и нейровоспаление. У людей было продемонстрировано, что воспаление потенцирует аммиак, провоцируя печеночную энцефалопатию, и что системное воспаление, а не аммиак, связано с тяжелой энцефалопатией.
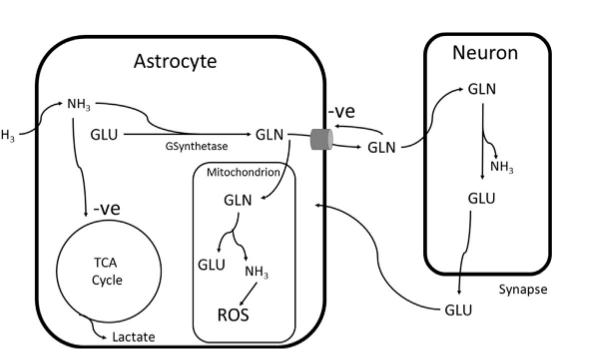
Изобр. 2. Представление о метаболизме аммиака в астроцитах и нейронах. В условиях гипераммонемии уровень глютамина повышается внутриклеточно, что приводит к окислительному повреждению митохондрий, а аммиак ингибирует цикл ТСА. Это нарушает клеточный метаболизм, что приводит к набуханию клеток. GLN, глутамин; GLU, глутамат; GS-синтетаза, глутаминсинтетаза; ROS, активные формы кислорода.
Аммиак и врожденная иммунная дисфункция.
Исследования i n vitro и in vivo показали, что фагоцитарная способность нейтрофилов снижается, а активность спонтанного окислительного взрыва возрастает при воздействии аммиака. Снижение фагоцитарной способности на фоне гипераммониемии также наблюдается у нейтрофилов собак in vitro. Это имеет важное значение, поскольку при высоких концентрациях аммиака повышается вероятность инфицирования и повышается активность спонтанного окислительного взрыва, усиливающего синдром воспалительной реакции.
Марганец
Марганец - необходимый микроэлемент, обладающий потенциальной нейротоксичностью, вызывает психические расстройства и когнитивные нарушения. Большая часть (98%) марганца, поступающего в организм и абсорбирующегося, эффективно удаляется печенью и выводится с желчью. Портосистемное шунтирование позволяет крови с высокой концентрацией марганца в висцеральном кровообращении поступать в системный кровоток. Астроциты обладают высокоаффинным механизмом переноса марганца, и его концентрация может быть в 50 раз выше, чем в окружающих клетках. Это приводит к окислительному повреждению и дисфункции митохондрий; было показано, что марганец вызывает астроцитоз Альцгеймера II типа, идентичный тому, что наблюдается при гипераммониемии.
Кроме того, марганец стимулирует микроглию к высвобождению воспалительных цитокинов и активных форм кислорода. Была продемонстрирована прямая взаимосвязь между содержанием марганца в крови, гиперинтенсивностью на сканах МРТ, соответствующей отложению марганца, и тяжестью печеночной энцефалопатии у людей. У собак с портосистемным шунтом и хроническими заболеваниями печени содержание марганца в крови выше, чем у контрольных животных. При проведении МРТ собак и кошек с портосистемным шунтом были обнаружены поражения центральной нервной системы, связанные с отложением марганца и есть одно сообщение о собаке с портосистемным шунтом, у которой при посмертном исследовании была повышена концентрация марганца в центральной нервной системе.
Кислотно-щелочные и электролитные нарушения
Гипонатриемия, гипокалиемия и алкалоз - все они, как известно, усиливают печеночную энцефалопатию у людей. Гипонатриемия усиливает отек мозга, в то время как гипокалиемия усиливает аммиакогенез в почках и снижает почечную экскрецию аммиака. Хотя вполне вероятно, что они также могут усиливать печеночную энцефалопатию у наших пациентов, доказательств этого недостаточно, и исследования, проведенные на сегодняшний день, не выявили никакой связи. Это может отражать низкую распространенность этих нарушений у наших пациентов, отчасти из-за различий в основной этиологии печеночной энцефалопатии (портосистемный шунт в сравнении с хроническим гепатитом) и тяжести патологического процесса; в случаях с хроническим гепатитом наши пациенты могут быть подвергнуты эвтаназии до того, как возникнут эти осложнения.
Неврологические последствия дисфункции астроцитов
При острой печеночной энцефалопатии основным патологическим последствием является отек мозга и повышение внутричерепного давления, вызванные увеличением астроцитов. При хронической печеночной энцефалопатии главным следствием всех этих факторов является нарушение регуляции нейромедиаторов. В дополнение к дисбалансу глутамата и глутаминового белка, при печеночной энцефалопатии уже давно был выявлен повышенный “ГАМКергический тонус”. G-аминомасляная кислота (ГАМК) является основным тормозящим нейромедиатором, снижающим возбудимость. Первоначально предполагалось, что это повышение тонуса вызвано повышенным cинтезом ГАМК; однако исследования на собаках с экспериментально индуцированным билиарным циррозом печени и собаках с экспериментально созданными портокавальными шунтами не выявили увеличения ГАМК или ГАМК-рецепторов центральной нервной системы. Это привело к поиску альтернативных лигандов.
В настоящее время известно, что ГАМК-рецепторы активируются группой соединений, известных как “ нейростероиды”, к которым относятся аллопрегнанолон и тетрагидродезоксикортикостерон. Было показано, что уровень этих соединений значительно повышается у людей с печеночной энцефалопатией. Нейростероиды синтезируются в ответ на активацию белка-транслокатора в митохондриях астроцитов (ранее известных как бензодиазепиновые рецепторы периферического типа). Количество этих рецепторов увеличивается у людей с циррозом печени. Исследования in vitro показали, что белок-транслокатор астроцитов в значительной степени регулируется аммиаком, а также марганцем.
Диагностика гепатоэнцефалопатии
Концентрация аммиака в артериях и венах является ненадежным показателем печеночной энцефалопатии. Следует поддерживать высокий индекс подозрительности у животных с заболеваниями печени или у тех, у кого может быть портосистемный шунт. Высокая концентрация аммиака делает вероятной печеночную энцефалопатию; однако нормальные значения не исключают этого диагноза. Во избежание повышения концентрации аммиака в пробирке важно тщательно обрабатывать пробы для определения содержания аммиака. Рутинная клиническая патология позволяет исключить другие метаболические причины неврологических заболеваний и позволяет выявить заболевания печени/ее недостаточность. Результаты визуализации брюшной полости могут подтвердить наличие приобретенных заболеваний печени и, в некоторых случаях, наличие системного шунтирования.
Продолжение статьи Печеночная энцефалопатия (гепатоэнцефалопатия) у собак и кошек. Часть 2